|
 |
DETERMINACIÓN DE MASAS ATÓMICAS Y MASAS MOLECULARES RELATIVAS |
 |
|
|
|
| |
|
La interpretación de los datos volumétricos
a la luz de la hipótesis de Avogadro permitió obtener fórmulas
correctas de muchos elementos y compuestos, evitando la regla de máxima simplicidad. Adicionalmente, la combinación de estos
conocimientos con los resultados del análisis químico también
sirvió para
obtener masas atómicas y masas moleculares relativas. |
| |
|
Síntesis
del cloruro de hidrógeno |
|
|
|
|
|
|
|
|
|
 |
 |
 |
|
 |
|
 |
|
1
vol. de hidrógeno |
|
1
vol. de cloro |
|
|
|
2
vol. cloruro de hidrógeno |
|
|
|
|
|
|
|
|
|
H2 |
+ |
Cl2 |
|
 |
|
2
HCl |
|
|
|
|
|
|
|
|
|
|
|
|
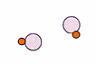
Veamos,
como ejemplo,
la reacción de síntesis del cloruro de hidrógeno,
representada en el esquema adjunto. Los resultados experimentales
sobre esta reacción informan de que cada gramo
de hidrógeno reacciona con 35,5 gramos de cloro. Por
tanto, como las moléculas de cloro y de hidrógeno
son ambas di-atómicas, se deduce que cada átomo de cloro
debería tener una masa 35,5 veces mayor que el de
hidrógeno.
La realidad es un poco más complicada.
En la naturaleza se encuentran
dos isótopos estables de cloro: uno 35 veces y el otro
37 veces más masivo que el hidrógeno. Estos isótopos
tienen unas proporciones relativas de 3:1
respectivamente, lo que da el resultado de una masa
atómica relativa para el cloro de 35,5. |
|
| |
|
De los datos de la reacción anterior también se deduce la
obviedad de que la molécula de hidrógeno gaseoso (H2)
tiene una masa doble que la del átomo de hidrógeno y que
la molécula de cloruro de hidrógeno (HCl) debería tener una masa
36,5 (35,5 + 1) veces mayor que la del átomo de hidrógeno.
|
| |
|
|
|
Dalton (entre
1803 y 1805), y
Berzelius
(entre 1808 y 1826), fueron los primeros en determinar masas
atómicas y masas moleculares relativas de bastantes
elementos conocidos. Dichas masas fueron definidas
inicialmente en relación al elemento más ligero, el
hidrógeno, al que se atribuyó en esta escala de masas
relativas el valor 1.
Posteriormente
Cannizzaro (1826-1910) refinó estos conceptos aplicando la hipótesis de Avogadro. En un Congreso celebrado en Karlsruhe en 1860,
formuló la siguiente ley para determinar las masas
atómicas de los elementos: las distintas cantidades
del mismo elemento contenido en distintas moléculas son
todas múltiplos enteros de la masa atómica.
Cannizzaro
(imagen a la izquierda de este texto) determinó experimentalmente masas atómicas y
masas moleculares comparando la densidad de vapor de un
conjunto de gases con moléculas conteniendo uno o más
átomos del elemento químico en cuestión. |
|
|
|
|
Sobre la base de
estos hallazgos y hasta mediados del siglo XX, los químicos y físicos utilizaron dos
escalas de masa atómicas relativas. Los químicos usaban una
escala tal que la mezcla natural de isótopos de oxígeno tenía
una masa atómica de 16, mientras que los físicos asignaron el
mismo número 16 a la masa atómica del isótopo de oxígeno más
común (oxígeno-16). Como en el oxígeno
natural están presentes el oxígeno-17 y el oxígeno-18, esto conducía a
2 tablas diferentes de masas atómicas relativas.
|
|
|
|
Entre 1959 y
1960 ambas organizaciones acordaron una escala unificada,
basada en el carbono-12 (el carbono-12 es el más abundante de
los dos isótopos estables del elemento carbono, representando el
98,89% de todo el carbono terrestre). Esta escala cumplía el
requerimiento de los físicos de basar la escala en un isótopo
puro y a la vez se hacía numéricamente cercana a la escala de
los químicos. Atendiendo a esta escala unificada se define: |
|
|
|
 |
|
|
Masa atómica
relativa: Número que indica cuántas veces mayor es la masa
de un átomo con respecto a 1/12 de la masa del isótopo del C-12.
|
| |
|
Masa
molecular relativa: Número que indica cuántas veces mayor es
la masa de una molécula de una sustancia con respecto a 1/12 de
la masa del isótopo del C-12. Se puede determinar sumando las
masas atómicas relativas de los elementos cuyos átomos
constituyen una molécula de dicha sustancia. |
|
|
|
|
|
La unidad de
masa atómica relativa y de masa molecular relativa se llama
Dalton o unidad de masa atómica y se abrevia u (antes uma).
|
|
| |
Índice |
 |
|
|
|
